Les maladies dites rares sont celles qui affectent moins d’une personne sur 2000. Si chacune de ces maladies peut être considérée comme « rare », prises ensemble les 7000 maladies rares identifiées concernent plus de trente millions de patients en Europe. Il y a environ 30.000 personnes touchées par une maladie rare au Luxembourg (ALAN-Maladies Rares Luxembourg). Presque 80% de ces maladies sont d’origine génétique et beaucoup affectent le cerveau. Même si les symptômes n’apparaissent pas toujours immédiatement, les maladies rares sont présentes tout au long de la vie des patients.
Les chercheurs du LCSB étudient plusieurs maladies rares dues à des mutations génétiques qui entrainent des symptômes chroniques graves. Pour pouvoir mettre au point de nouveaux traitements, il est essentiel d’identifier les causes génétiques et de comprendre les mécanismes moléculaires responsables de chaque maladie.

Dr Carole Linster et ses collaborateurs ont récemment identifié la cause génétique d’une nouvelle maladie infantile grave. Les enfants touchés par cette maladie – un déficit en enzyme NAXD – souffrent généralement d’épisodes de régression neurologique, déclenchés par une fièvre ou une infection, et présentent différents symptômes, comme des lésions cutanées et une neurodégénérescence, entraînant un décès précoce. Les chercheurs ont découvert que NAXD est ce que l’on appelle un enzyme de réparation. Il a pour rôle d’éliminer des substances issues du métabolisme qui ne sont pas utilisés par l’organisme et peuvent devenir toxiques. Chez les patients, cet enzyme ne fonctionne pas correctement. Par conséquent, les substances toxiques s’accumulent dans les cellules et les abîment. L’équipe de recherche souhaite maintenant importer la mutation génétique responsable chez des poissons-zèbres et dans des cultures de cellules nerveuses dérivées à partir de cellules-souches de patients. L’objectif est de recréer la maladie dans ces modèles au laboratoire afin de mieux comprendre comment elle se développe et de commencer à tester des approches thérapeutiques.
L’équipe étudie aussi d’autres maladies rares grâce à différents organismes modèles comme les levures et les poissons-zèbres. Cela permet notamment de passer au crible de nombreuses petites molécules et de déterminer si elles pourraient être utilisées pour modifier le cours de la maladie. Saviez-vous que les levures de boulanger, celles qui servent à faire le pain ou la bière, possèdent des gènes en commun avec les humains, y compris jusqu’à 30% de ceux connus pour leur rôle dans des maladies ? Au laboratoire, il est donc possible d’introduire une mutation observée chez un patient dans le gène correspondant chez la levure, et de reproduire ainsi la maladie dans l’organisme modèle pour l’étudier plus facilement.
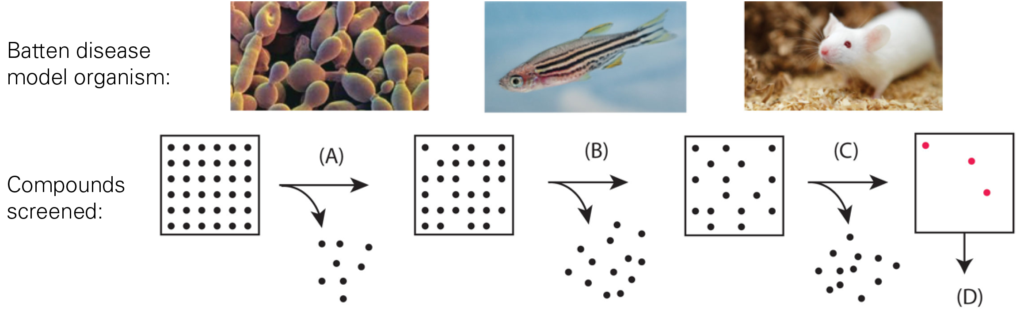
C’est ce qui a été fait dans le cas de la maladie de Batten par exemple. Il s’agit du trouble neurodégénératif infantile héréditaire le plus courant. Des mutations au niveau du gène ATP13A2, qui est aussi impliqué dans une forme juvénile de la maladie de Parkinson, déclenchent des convulsions, des changements de personnalité et de comportement, des problèmes moteurs et des troubles du langage chez les enfants. Il n’existe actuellement aucun traitement efficace pour cette maladie mortelle. En testant des centaines de molécules chez des levures et des poissons-zèbres porteurs des mêmes mutations, les chercheurs du LCSB ont récemment identifié deux substances prometteuses – dont une déjà utilisée en tant que médicament pour d’autres maladies humaines. Ces substances permettent d’inverser l’effet des mutations responsables de la maladie de Batten chez les poissons et les levures. La prochaine étape est d’étudier leur efficacité chez les souris, avant de pouvoir les tester chez les patients atteints de la maladie de Batten.
L’équipe vient également de lancer un projet de recherche sur le syndrome de Zellweger, une maladie qui affecte la biogénèse des peroxysomes. Du fait de la dégradation de la fonction peroxysomale, les patients accumulent de très longues chaines d’acides gras et des acides gras ramifiés qui sont normalement dégradés dans les peroxysomes. L’accumulation de ces lipides peut affecter le fonctionnement de multiples organes, entrainant par exemple un retard dans le développement cérébral, des convulsions, une faiblesse musculaire et un dysfonctionnement du foie.
L’industrie pharmaceutique investit assez peu dans la mise au point de traitements pour les maladies rares du fait du faible nombre de patients affectés par chaque maladie. Nous sommes donc très reconnaissants du soutien financier que nous avons reçu de la part de diverses sources. Nous souhaitons particulièrement remercier le Fonds national de la recherche (FNR), l’université de Luxembourg, la fondation ATOZ, la fondation LOSCH, la fondation Juniclair, le Lions club, le Rotary club, l’Association luxembourgeoise des amis de la fondation Louvain, ainsi que différents mécènes privés.
La Professeure assistante Carole Linster et son équipe, le groupe Enzymology & Metabolism, étudient plusieurs maladies rares causées par des mutations génétiques et entraînant des symptômes chroniques et potentiellement mortels. Pour développer de nouveaux traitements, il est important de déterminer la cause génétique et de comprendre les mécanismes moléculaires qui sous-tendent la maladie.
La maladie neurodégénérative héréditaire la plus fréquente chez les enfants est basée sur des mutations du gène ATP13A2, qui est également impliqué dans une forme juvénile de la maladie de Parkinson. Elle déclenche des crises d’épilepsie, des changements de personnalité et de comportement, des problèmes d’élocution et de motricité chez les enfants. Il n’existe actuellement aucune option de traitement efficace pour cette maladie mortelle. Après avoir testé des centaines de molécules dans les modèles de levure et de poisson zèbre de la « maladie de Batten », les chercheurs du LCSB ont trouvé deux médicaments, dont l’un est déjà utilisé chez l’homme pour d’autres maladies, et qui ont inversé l’effet des mutations de la maladie de Batten dans les modèles de levure et de poisson. Dans une prochaine étape, l’efficacité de ces médicaments doit être étudiée chez la souris avant de pouvoir être testée chez les patients atteints de la maladie de Batten.
En raison de l’altération de la fonction des peroxysomes, les patients atteints du syndrome de Zellweger accumulent des acides gras à très longue chaîne et des acides gras à chaîne ramifiée qui sont normalement dégradés dans les peroxysomes. L’accumulation de ces lipides peut altérer le fonctionnement normal de plusieurs systèmes organiques, entraînant par exemple des troubles du développement cérébral, des crises d’épilepsie, une diminution du tonus musculaire et un dysfonctionnement du foie.
Les enfants touchés par cette maladie – un déficit en enzyme NAXD – souffrent généralement d’épisodes de régression neurologique, déclenchés par une fièvre ou une infection, et présentent différents symptômes, comme des lésions cutanées et une neurodégénérescence, entraînant un décès précoce. Les chercheurs ont découvert que NAXD est ce que l’on appelle un enzyme de réparation. Il a pour rôle d’éliminer des substances issues du métabolisme qui ne sont pas utilisés par l’organisme et peuvent devenir toxiques. Chez les patients, cet enzyme ne fonctionne pas correctement. Par conséquent, les substances toxiques s’accumulent dans les cellules et les abîment. L’équipe de recherche souhaite maintenant importer la mutation génétique responsable chez des poissons-zèbres et dans des cultures de cellules nerveuses dérivées à partir de cellules-souches de patients. L’objectif est de recréer la maladie dans ces modèles au laboratoire afin de mieux comprendre comment elle se développe et de commencer à tester des approches thérapeutiques.
© 2026 LCSB Fundraising
Notices légales
Design by marcwilmes.com
